مولکول چیست

در این مقاله توضیح میدهیم که مولکول چیست. همچنین به انواع مولکولها و تفاوت مولکول با ترکیب شیمیایی اشاره خواهیم کرد.
مولکول چیست؟
به دو یا چند اتم که بینشان پیوند شیمیایی برقرار است، مولکول میگویند. بعضی از مولکولها اتمهای همسان و برخی دیگر اتمهای متفاوتی دارند. مثلا مولکول هیدروژن (H۲) از دو اتم همسان هیدروژن تشکیل شده است. اما مولکول آب (H۲O) حاوی دو نوع اتم متفاوت یعنی هیدروژن و اکسیژن است. ترکیبهای شیمیایی نیز در اصل نوعی مولکول هستند که در ساختارشان اتمهای بیش از یک عنصر بهکار رفته است. مولکولها در اثر پیوند شیمیایی اتمها بوجود میآیند. در ادامه با جزییات بیشتری بررسی میکنیم که مولکول چیست، تفاوت مولکول با ترکیب چیست و مولکولها چه انواعی دارند. پیش از پرداختن به مبحث مولکول، بهتر است ابتدا چهار مفهوم بنیادی را در اینخصوص مرور کنیم:
- اتم: به کوچکترین جزء یک عنصر که خواص آن عنصر را داراست، اتم میگویند. تعداد پروتونهای موجود در هسته هر اتم، ماهیت آن اتم را مشخص میکند و نشان میدهد که آن اتم متعلق به چه عنصری است. برای مثال، هر اتمی که در هسته خود تنها یک پروتون داشته باشد، قطعا اتم هیدروژن است و اگر ۲ پروتون داشته باشد قطعا اتم هلیوم است.
- عنصر شیمیایی: مادهای است که تمام اتمهای سازنده آن یکسان و متعلق به همان عنصر است. برای مثال، نقرهی خالص تماماً از اتمهای نقره تشکیل شده است. بههمین سبب خواص شیمیایی هر عنصر دقیقا شبیه خواص شیمیایی اتمهای آن عنصر است. اکسیژن، هیدروژن، نقره، مس، طلا و اورانیوم تنها چند نمونه از عناصر شیمیایی هستند.
- مولکول: همانطور که گفتیم، وقتی اتمهای یک یا چند عنصر با پیوند شیمیایی به هم متصل شوند، مولکول میسازند. برای مثال، وقتی دو اتم اکسیژن با هم پیوند شیمیایی ایجاد کنند، مولکول اکسیژن (O۲) میسازند. یا چنانچه دو اتم هیدروژن با یک اتم اکسیژن پیوند شیمیایی ایجاد کند، مولکول آب (H۲O) میسازد.
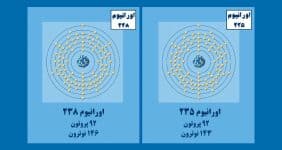
مطلب مرتبط: ایزوتوپ چیست؟
تفاوت ترکیب و مولکول چیست
هر ترکیب شیمیایی در اصل نوعی مولکول است. به مولکولهایی که از اتصال اتمهای بیش از یک عنصر پدید آمده باشند، ترکیب میگویند. برای مثال، مولکول آب (H۲O) حاصل پیوند اتمهای دو نوع عنصر متفاوت یعنی اکسیژن و هیدروژن است، و لذا ترکیب محسوب میشود. اما موکول هیدروژن (H۲) فقط یک مولکول است و ترکیب بهشمار نمیرود. توجه داشته باشیم که همه ترکیبها مولکول هستند اما هر مولکولی ترکیب نیست.

گفتیم که مولکول حاصل پیوند شیمیایی دو یا چند اتم است. پس لازم است ابتدا بدانیم که پیوند شیمیایی چیست و سپس انواع پیوندهای شیمیایی بین اتمها را خلاصهوار مرور کنیم.
مطلب مرتبط: آفتابپرست چگونه رنگ عوض میکند؟
انواع پیوندهای شیمیایی
پیوند شیمیایی نیرویی است که اتمها، یونها و مولکولها را کنار هم نگه میدارد. با پیوند اتمها به یکدیگر مولکول تشکیل میشود و از پیوند مولکولها با هم ترکیبهای شیمیایی شکل میگیرند. تعداد الکترونهای موجود در لایههای اتم بهویژه تعداد الکترونهای موجود در لایه ظرفیت اتم در نحوه پیوند آن اتم با اتمهای دیگر نقش مهمی دارد. گاهی نیروی جاذبه الکترواستاتیک بین یونهای با بار مخالف سبب ایجاد پیوند یونی میشود. گاهی نیز دو اتم الکترونهایشان را به اشتراک مینهند و بدینسبب به هم پیوند میخورند که به آن پیوند کووالانسی میگویند. پیوندهای شیمیایی چند نوعند که رایجترین آنها چنین هستند:
- پیوند یونی
- پیوند کووالانسی
- پیوند فلزی
- پیوند هیدروژنی
پیوند یونی
در پیوند یونی، یک یا چند الکترون تماماً از اتم یک عنصر به اتم عنصر دیگر منتقل میشوند. نیروی جاذبه ناشی از قطبش بارهای الکتریکی مخالف، اتمهای آن عناصر را کنار هم نگه میدارد. پیوند یونی بین عناصری که اختلاف الکترونگاتیو بزرگی دارند معمولتر است. مثال:
- نمک یا کلرید سدیم (NaCl)
پیوند کووالانسی
در پیوند کووالانسی، دو اتم الکترونهای لایه ظرفیت خود را به اشتراک مینهند و بدینوسیله با هم پیوند ایجاد میکنند. وقتی یک اتم برای کامل کردن لایه ظرفیتش الکترون بخواهد، الکترونهای لایه ظرفیت خود را با اتم دیگر به اشتراک مینهد و اتم مجاور نیز همین کار را انجام میدهد. نتیجتا این الکترونهای مشترک لایههای ظرفیت هر دو اتم را پر میکنند. مثال:
- گاز یُدین (I۲): از پیوند دو اتم یدین (I)، گاز یدین حاصل میشود.
- دیاکسید کربن (CO۲): دو اتم اکسیژن و یک اتم هیدروژن با پیوند کووالانسی دوگانه، مولکول دیاکسید کربن میسازند.
- مولکول آب (H۲O): دو اتم هیدروژن و یک اتم اکسیژن با ایجاد پیوند کووالانسی قطبی، مولکول آب میسازند.
- بوران (BH۳): سه اتم هیدروژن با یک اتم بور، پیوند کووالانسی قطبی ایجاد میکنند و مولکول بوران (تریهیدروبورون) تشکیل میدهند.
پیوند فلزی
در پیوند فلزی، اتمها نه الکترون به اشتراک مینهند و نه الکترون مبادله میکنند، بلکه هر اتم یک یا چند الکترون خود را آزاد میکند و بدینسان انبوهی از الکترونهای آزاد در فلز به حرکت درمیآیند. لذا هر الکترون میتواند با الکترونهای متعددی از اتمهای ثابت تعامل و پیوند ایجاد کند. مثال:
- فلز سدیم
- ورق یا فویل آلومینیومی
- سیم مسی
پیوند هیدروژنی
پیوند هیدروژنی، هم میتواند درونمولکولی و هم بینمولکولی باشد؛ یعنی هم بین اجزای یک مولکول و هم بین مولکولهای جداگانه ایجاد شود. این نوع پیوند در اصل نیروی جاذبه الکترواستاتیک بین یک اتم هیدروژن است که بصورت کووالانسی به یک اتم یا به گروهی از اتمها با الکترونگاتیوی بیشتر متصل است. مثال:
- اتم هیدروژن موجود در یک مولکول آب با اتم اکسیژن موجود در مولکول دیگر آب بوسیله پیوند هیدروژنی بههم متصل میشوند.
- در مولکول کلروفورم (CH۳Cl) و مولکول آمونیاک (NH۳)، پیوند هیدروژنی بین اتم هیدروژن یک مولکول و اتم کربن یا نیتروژن مولکول دیگر شکل میگیرد.
- بازهای نیتروژنی موجود در دیانآ (DNA) بوسیله پیوند هیدروژنی شکل میگیرند.
قوت و ضعف پیوندهای شیمیایی با هم فرق دارد. پیوند یونی، کووالانسی و فلزی در زمره پیوندهای اصلی و قوی هستند. مولکولهای جامدات بسیار نزدیک هم به یکدیگر پیوند خوردهاند. وقتی جاذبه بین آنها ضعیفتر شود، ماده از جامد به مایع تغییر حالت میدهد. وقتی ماده به حالت گاز درمیآید، بین اتمها یا مولکولهای آن تقریبا هیچ پیوندی وجود ندارد و این ذرات آزادانه و مستقل از یکدیگر در محیط حرکت میکنند.
مطلب مرتبط: چگالی ماده چیست و چگونه محاسبه میشود؟
انواع مولکولها
مولکولها را برپایه تعداد اتمهایشان میتوان به چند دسته تقسیم کرد:
- مولکولهای دو اتمی (diatomic molecules)
- مولکول دو اتمی با اتمهای همسان: مثل H۲، O۲ و N۲
- مولکول دو اتمی با اتمهای ناهمسان: مثل مونوکسید کربن (CO)
- مولکولهای سهاتمی (triatomic molecules)
- مولکول سهاتمی با اتمهای همسان: مثل مولکول اوزون (O۳)
- مولکول سهاتمی با اتمهای ناهمسان: مثل مولکول آب (H۲O)، دیاکسیدکربن (CO۲) و هیدروکسیدپتاسیم (KOH)
- مولکولهای چنداتمی (polyatomic molecules)
- مولکولهای سه یا بیش از سه اتم دارند را میتوان در زمره مولکولهای چنداتمی جای داد. در اینصورت مولکول آب و مولکول اووزن نیز در این دسته جای میگیرند. و البته مولکولهایی با اتمهای بسیار بیشتر مثل هگزافلوراید اورانیوم (UF۶) نیز در این دسته هستند.
مطلب مرتبط: پلاسما چیست و با گاز چه تفاوتی دارد
اندازه مولکول
اندازه مولکول به نوع آن بستگی دارد. برای مثال قطر هر مولکول ساده آب شامل ۲ اتم هیدروژن و یک اتم اکسیژن تنها ۰.۲۷ نانومتر است. با استفاده از فناوری نانو میتوان بعضی از ساختارهای مولکولی و اتمی را تغییر داد و مواد جدیدی تولید کرد و یا مواد موجود را بسته به نیازها بهبود داد.
جمعبندی: مولکول چیست و چه انواع و چه ویژگیهایی دارد
به اتمهایی که بوسیله پیوند شیمیایی کنار هم جای گرفته باشند، مولکول میگویند. سادهترین مولکولها حداقل دو اتم دارند. اتمهای مولکول ممکن است همسان یا ناهمسان باشند. به مولکولی که در ساختار خود بیش از یک نوع عنصر داشته باشد، ترکیب میگویند فلذا همه ترکیبها در اصل نوعی مولکول هستند. پیوندهای شیمیایی انواع مختلفی دارند اما پیوند یونی، پیوند کووالانسی، پیوند فلزی و پیوند هیدروژنی در مواد مختلف معمولترند.